在生物制藥領域,無菌過濾工藝是確保最終產品質量和安全性的關鍵環節之一。其中,用于去除細菌和控制生物負荷的除菌過濾系統一直是無菌過濾工藝中的重要環節。
PUPSIT定義
根據EU 新版 GMP 的相關規定“8.87 The integrity of the sterilised filter assembly should be verified by integrity testing before use (pre-use post sterilisation integrity test or PUPSIT), to check for damage and loss of integrity caused by the filter preparation prior to use.”
PUPSIT,即“使用前、滅菌后完整性測試”(Pre-Use Post-Sterilization Integrity Test),是無菌制藥工藝中的一項重要測試措施。
由于滅菌過程可能會對過濾器產生影響,如導致微小破損、孔徑變化,或引入“掩蓋缺陷”的風險,PUPSIT幫助制藥企業在生產啟動之前確認過濾器是否能有效地過濾微生物和其他顆粒,確保產品的最終無菌性。
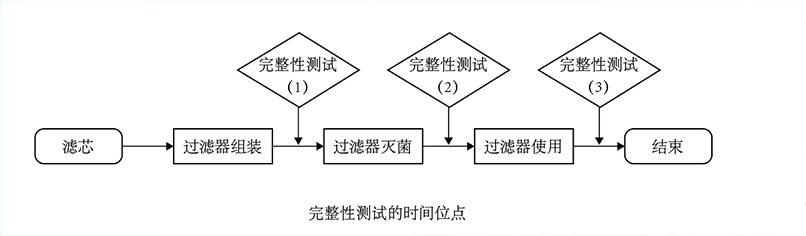
實施要點
1. 測試時機與流程設計
嚴格時序:必須在過濾器完成滅菌(如濕熱滅菌、輻照滅菌)后,且在實際使用(如藥液過濾、無菌工藝)前進行,避免滅菌后二次污染或操作損傷。
無縫銜接:若滅菌后無法立即測試(如過濾器已安裝于系統),需確保測試前系統處于密閉狀態,防止外界污染。
2. 滅菌方法兼容性
濕熱滅菌(SIP):需驗證高溫高壓對濾膜(如PES、PVDF)的影響,避免膜孔徑變形或密封件老化。
輻照滅菌:注意γ射線或電子束可能降低濾膜機械強度,需通過完整性測試確認無損傷。
環氧乙烷(EO)滅菌:需徹底解析殘留氣體,避免影響測試結果(如擴散流測試干擾)。
3. 完整性測試方法選擇
起泡點測試(Bubble Point):適用于膜孔徑較大(≥0.2μm)的除菌過濾器,需設定滅菌前后的閾值(如0.2μm濾膜起泡點≥3.5 bar)。
擴散流/前進流測試(Diffusion Flow):更敏感,適用于小孔徑或多層濾膜,需根據濾膜材質和滅菌條件校準標準值。
壓力衰減測試(Pressure Hold):適用于在線測試,需確保系統密閉性(如管路、接頭無泄漏)。
4. 測試系統設計
在線測試 vs. 離線測試:
在線測試:直接在生產系統中進行,需驗證測試設備(如完整性測試儀)與工藝管路的兼容性。
離線測試:適用于小型或獨立過濾器,需確保拆卸-測試-重新安裝過程的無菌性。
自動化集成:優先采用自動化測試設備,減少人為操作誤差,確保數據完整性(如電子記錄符合ALCOA+原則)。
5. 驗證與接受標準
滅菌前后對比:需建立滅菌前(出廠)與滅菌后(PUPSIT)的完整性測試數據基線,確認滅菌過程未導致性能漂移。
接受標準:依據過濾器廠家標定值,結合工藝驗證數據設定(如擴散流≤10 mL/min·cm2)。
失敗處理:若測試失敗,需啟動偏差調查(是否為滅菌損傷、安裝不當或測試誤差),并更換過濾器。
風險評估與關鍵控制
風險點:滅菌參數超限(如溫度過高)、過濾器安裝不當(如O型圈損壞)、測試環境(如非潔凈區操作)。
控制措施:通過工藝驗證(如滅菌循環驗證)、操作SOP培訓、環境監控(如粒子計數)降低風險。
法規與文件要求
GMP/FDA合規:符合FDA《無菌工藝指南》、EU GMP Annex 1(2022)要求,明確PUPSIT為強制步驟。
?歐盟GMP附錄1:2022年發布的新版附錄1明確要求,在沒有顯著工藝限制(如溶液體積較小)的情況下,制藥企業必須在使用前對滅菌后的除菌過濾器進行PUPSIT測試。這不僅是為了防止微生物污染,還因滅菌過程可能導致濾器的完整性下降,從而影響藥品的無菌質量。
?美國FDA:FDA的相關指南雖然未明確要求所有情況下必須執行PUPSIT,但強調根據產品特性進行風險評估,并在必要時執行完整性檢測。對于那些無法在滅菌后實施PUPSIT的產品,需基于科學依據采取其他風險控制措施。
?WHO和PIC/S:全球化的GMP指南如WHO和PIC/S同樣支持PUPSIT,特別是針對出口或跨國銷售的無菌藥品,要求嚴格執行PUPSIT的流程,以確保最終產品質量達到國際標準。

文件記錄:需完整記錄滅菌參數、測試結果、操作人員、設備編號等信息,支持產品批次放行。
審計重點:檢查測試數據趨勢分析、偏差記錄、過濾器更換頻率是否合理。
典型案例應用
注射液除菌過濾:在線PUPSIT確保藥液過濾前過濾器完整性。
生物反應器進氣過濾器:滅菌后測試防止細胞培養污染。
無菌包裝器械:測試呼吸袋過濾器是否在EO滅菌后仍維持無菌屏障。
總結
PUPSIT是保障無菌工藝安全的核心環節,需通過科學的驗證、嚴格的流程控制和合規的文件管理實現。實施時應結合具體工藝特點(如滅菌方式、過濾器類型),確保測試結果的可靠性與重現性。